Competitive GPCR-targeted antibody pipelines generated from
MoGRAA® Discovery Engine
MoGRAA®ディスカバリーエンジンから生み出される競争力のあるGPCR標的抗体パイプライン
Advantages of MoGRAA® Antibody- MoGRAA®抗体の優位性
MoGRAA® Discovery Engine is our proprietary drug discovery platform specialized for GPCR-targeted antibodies. Our pipeline, powered by MoGRAA® discovery engine, has a competitive advantage over conventional GPCR-targeted drugs.
当社独自のGPCR標的抗体に特化した創薬探索プラットフォーム「MoGRAA®ディスカバリーエンジン」。MoGRAA®ディスカバリーエンジンを応用し生み出される当社のパイプラインは、従来型のGPCR標的薬と比較し、競争優位性を有しています。
| MoGRAA® antibody | Conventional GPCR Drug | |
| Drug type | Monoclonal antibody | Small molecule or peptide |
| Mode of action | Antagonist, Agonist, Modulator | Antagonist, Agonist, Modulator |
| Duration of action | Long | Short |
| Selectivity | High | Moderate |
| Off-target | Low frequency | High frequency |
| ADME profile | Relatively simple | Complicated (depend on chemical property) |
| Biomarker survey | Good as diagnostic tool | New tools needed |
| Period of drug discovery | Short | Relatively long |
| Drug Cost | Middle-High | Low-Middle (Molecular Targeting Drugs) |
Pipelines of GPCR-Targeted Antibody-GPCR標的抗体パイプライン
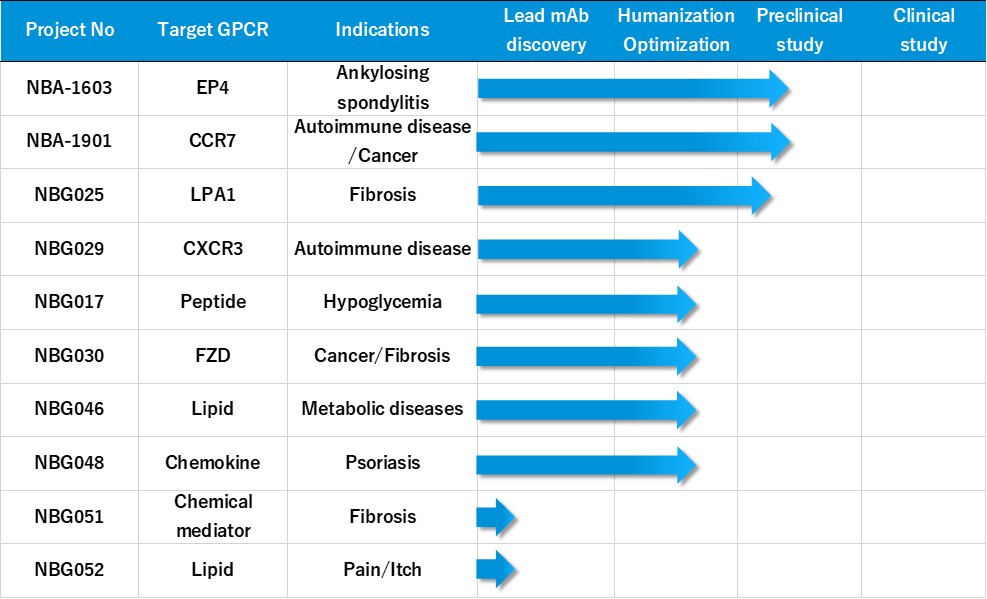
Focus Therapeutic Areas – 重点疾患領域
We have positioned the following diseases as our focal therapeutic areas and are developing them in-house.
当社では、以下の疾患を重点疾患領域と位置づけ、自社開発を進めています。
Fibrosis – 線維症
Fibrogenesis is a process of wound healing, but after repeating this process, the tissue becomes stiff and abnormal function, resulting a disease called fibrosis. Fibrosis can occur in various organs, but fibrosis in the lung, liver, and kidney is serious, therefor, promising therapeutic drugs is strongly desired.
線維化は、組織が損傷を受けた際に起こる、創傷治癒の過程ですが、この過程を繰り返すと、組織が硬くなり、正常な働きができなくなる線維症という疾患となります。線維症は様々な臓器で起こり得ますが、特に肺や肝臓、腎臓における線維症は重篤であり、有用な治療薬の開発が強く望まれています。
NBHL is currently developing two therapeutic mAbs for Fibrosis.
現在、当社では線維症を対象とした2つの治療用モノクローナル抗体を開発中です。
NBA-1901:CCR7 selective monoclonal antibody – CCR7選択的モノクローナル抗体
Project NBA-1901 is a first-in-class therapeutic mAb targeting a chemokine receptor involved in the tissue fibrosis pathway. The mAb exerts a therapeutic effect by shutting down chemokine-induced GPCR signaling. Using the surrogate mAb for the rat homologue of the target GPCR, we proved the therapeutic concept of the antibody treatment in a lung fibrosis model, with superiority over the existing small molecule drug for IPF. The mAb for the chemokine receptor also has a potential application for kidney fibrosis. NBHL is now progressing with the optimization of humanized antibodies ready for preclinical development for Idiopathic pulmonary fibrosis.
NBA-1901は、組織線維症に関与しているケモカインGPCRをターゲットとするFirst in classの治療用モノクローナル抗体です。この抗体がCCR7に結合すると、 細胞内のシグナル伝達経路を完全阻害することで治療効果を発揮します。
CCR7は肺線維症の一種である、特発性肺線維症(IPF)に関与していることが示唆されています。当社では、肺線維症モデルにおける治療コンセプトを検証済みであり、他にも腎線維症に対する適応の可能性を示すデータも得ています。現在、肺線維症の一つである特発性肺線維症(IPF)での前臨床試験に向け、製造検討を進めています。
NBG025:LPA1 selective monoclonal antibody – LPA1選択的モノクローナル抗体
A proprietary first-in-class therapeutic monoclonal antibody targeting LPA1, a lipid mediator receptor associated with tissue fibrosis, was created. When this antibody binds to LPA1, it is expected to have a therapeutic effect by completely inhibiting the intracellular signaling pathway.
LPA1 is thought to be involved in idiopathic pulmonary fibrosis (IPF), one type of tissue fibrosis, and human clinical studies of LPA1 small molecule inhibitors for IPF are underway. We have also obtained promising therapeutic efficacy data of this antibody in a mouse model of pulmonary fibrosis and are currently conducting pre-clinical studies of this antibody.
組織線維症に関与している脂質メディエーターの受容体LPA1をターゲットとするFirst in classの治療用モノクローナル抗体を創製しました。この抗体がLPA1に結合すると、 細胞内のシグナル伝達経路を完全阻害することで治療効果を発揮することが期待されます。
LPA1は臓器の線維症の一種である特発性肺線維症(IPF)に関与していることが示唆されており、LPA1低分子阻害剤を用いたIPFでのヒト臨床試験が進行中です。当社では、マウスを用いた肺線維症モデルの試験において治療効果を示す有望なデータも得ており、前臨床試験を進めています。
Autoimmune disease – 自己免疫疾患

Autoimmune diseases occur when the body’s own immune cells misidentifies, then attacks its own organisms. Various GPCRs (chemokine receptors, lipid-related receptors) work in concert with cytokines and adhesion molecules to promote activation of Th17 cells and dendritic cells, which are the causative cells of autoimmune diseases and chronic inflammation, and consequently thought to be involved in chronic inflammation.
自己免疫疾患は、自分の体が免疫系細胞により異物として誤認され、攻撃されることによっておこる疾患です。様々なGPCR(ケモカイン受容体、脂質関連受容体)が、サイトカインや接着分子と協調して自己免疫疾患や慢性炎症の原因細胞であるTh17細胞や樹状細胞の活性化を促進し、結果的に慢性炎症に関与していると考えられています。
Prostaglandin E2 receptor subtype, EP4, is thought to be involved in chronic inflammation. No small molecule drug targeting EP4 is available owing to the problems with off-target effects, etc.
The EP4 antibody treatment has its advantages compared with small molecule drugs in terms of its receptor subtype selectivity, limited distribution, and long duration.
In recent years, it has been reported that there is a correlation between the severity of ankylosing spondylitis and EP4 expression. It is expected to be a diagnostic and therapeutic agent for Ankylosing Spondylitis as well, in addition to therapeutic agents for autoimmune diseases such as colitis, psoriatic arthritis.
GPCRの1つである、EP4(プロスタグランジンE2受容体サブタイプ4)は慢性炎症に関与していると考えられています。EP4を標的とした低分子医薬品の開発も行われてきましたが、オフターゲット効果などの問題で未だ上市には至っていません。
EP4抗体治療は、受容体サブタイプ選択性、限定された分布、長い持続時間という点で、低分子医薬品と比較して利点があります。
近年、強直性脊椎炎の重症度とEP4発現量に相関があることが報告されています。大腸炎、関節症性乾癬などの自己免疫疾患の治療薬に加え、強直性脊椎炎の診断薬・治療薬としても期待されています。
NBA-1603:EP4 selective monoclonal antibody – EP4選択的モノクローナル抗体
NBHL’s anti-human EP4 antibody, NBA-1603 is a first-in-class EP4 receptor selective antibody. It fully antagonizes EP4-dependent cAMP elevation and beta-arrestin activity without antibody-dependent cellular cytotoxicity (ADCC) or complement-dependent cytotoxicity (CDC). The antibody has been shown to inhibit EP4-dependent cAMP elevation and modulate IL-17 production in human primary CD4+ T cells. NBHL is currently optimizing the antibody for preclinical testing.
NBA-1603は、ファーストインクラスのEP4受容体選択的モノクローナル抗体です。抗体依存性細胞傷害(ADCC)や補体依存性細胞傷害(CDC)を引き起こさず、この抗体はEP4による細胞内へのシグナル伝達系を完全に阻害します。さらにヒト細胞において、サイトカインIL-17の産生を調節する結果が得られています。現在、前臨床試験に向けた抗体の最適化を行っています。
Severe virus infections – 重症ウイルス感染症

For the purpose of severe viral infection control such as influenza and COVID-19, we focus on events caused by viral infections on the “human (host)” instead of the “viruses itself” as therapeutic targets. Based on the concept, we are aiming for anti-severe viral infection drug development.
We have discovered several common pathways contributing to viral infection severity by using omics data derived from mouse models of severe influenza. In these pathways, some GPCRs, such as chemokine receptors, lipid mediator receptors, and nucleic acid receptors, have been identified as target candidates in these pathways. We are now searching for and optimizing lead monoclonal antibodies by the MoGRAA® Discovery Engine and also pursuing POC evaluation.
We expect that the development of therapeutic drugs that target the host might contribute to the treatment of severe viral infection symptoms regardless of the type of virus.
インフルエンザやCOVID-19などのウイルス感染による重症化の治療を目的に、治療標的として、『ウイルス』ではなく『ヒト(宿主)』側のウイルス感染により引き起こされるイベントに着目し、重症ウイルス感染症治療薬の開発を目指しています。
当社は、重症インフルエンザマウスモデルを用いてオミックス情報を取得し、ウイルス感染症の重症化に共通の標的パスウェイを複数見出してきました。それらのパスウェイにはケモカイン受容体や脂質メディエーターの受容体、核酸受容体など複数のGPCRが標的候補として見出されており、現在、コンセプト検証と並行してMoGRAA®ディスカバリーエンジンを応用して治療用リードモノクローナル抗体の探索と最適化を進めています。
宿主を標的とする治療薬の開発は、病因であるウイルスの種類によらず、重症化の治療に貢献できる可能性があると期待しています。